新闻中心
制药的未来是模块化制造吗?
一场 ISPE Pharma 4.0 与 GAMP 实践社区成员间关于生命科学行业是否采用模块化自动化工厂的主题讨论。
在当今节奏的制药环境中,行业内的各家企业需要不断努力提高工艺效率、提高灵活性和加快药品的上市时间。这使得是否能够实现其生产自动化车间内的设备更快、更顺畅系统集成的能力至关重要。而达成上述目标的方法之一是被人称之为模块类型化(MTP)的模块化自动化方法,它可以支持这一过程的实现。
虽然像 NAMUR 和 Profibus Profinet 国际用户 组织(PI)等国际标准化机构仍然会继续在这一领域中发挥重要作用,同时也有许多工业团体正在积极探索如何将 MTP 技术应用于生命科学行业。他们的关注点在哪里?答案就是关于如何简化和加速资格认证和验证过程。
为此我有和同在 ISPE Pharma 4.0 Plug & Produce 团队的二位同事 Rod Hoffman 、Thomas Makait 就此彼此就“模块化自动化如何彻底改变药品制造的未来”进行了交流与沟通。

罗德·霍夫曼
Rod Hoffman 常驻特拉华州威尔明顿,在阿斯利康工作了近 20 年,在制造、运营和 IT 领域担任过关键职务。Rod 目前是 IT 工程能力总监,专门从事 IT/OT 集成,专注于使技术与业务需求保持一致,以提高运营效率。
Giuseppe Menin:Rod,模块化自动化主要可以带给像阿斯利康这样的制药企业带来哪些好处?
Rod Hoffman:当我在阿斯利康负责MES实施平台的工作后,我清楚地意识到了模块化应用的优势。将企业纸质生产批次数据记录转为电子文档记录生产批次(EBR)是实现生产数据标准化的重要举措之一。 虽然整个企业的众多业务相关部门都为能将车间生产设备(ISA 95 Lev. 2)数据集成到 MES 平台 (ISA 95 Lev. 3)而感到兴奋。且在公司业务层面的一些站点已完全采用了面板展示信息的方式。但是我很快意识到我们的系统缺乏标准化。这意味着每个工作站点都以不同的方式集成其设备,尽管其中大部分通常会采用 OPC DA 或 HDA 等经典技术。换句话说,我们的工程师必须从头开始设计每个接口,这需要大量的验证文档,由于缺乏接口标准化,这些文档很少可以被重复使用。
正是在那时,我们的 MES 供应商开始寻找使用基于消息的方法来简化集成的方法,这就是我的模块化自动化之旅的开始。集成车间设备的好处对我来说已经很清楚了。现在,我也明白,如果没有标准化,从长远来看,这种整合过程的维持成本将很高。我认为 MTP 是一项很有前途的技术,可以支持标准化并随着时间的推移降低集成成本,同时使阿斯利康等公司能够充分实现集成的好处。从本质上讲,这一切都是为了无缝连接设备,以便我们可以轻松访问所需的数据并推动价值的增加。
Giuseppe Menin:MTP 在制药行业的哪些领域被证明特别有效?MTP 是否可以帮助解决与新型或新兴应用集成这类挑战?
Rod Hoffman: 我们在多个领域上真正看见了这种机会——例如在我们最近建造的细胞生成与基因治疗工厂上。此类新工厂应用系统是 MTP 的完美匹配者。虽然我们企业所使用的大多数设备的供应商尚未采用 MTP,但我相信,一旦他们意识到这种方法对他们有多么有益,他们就会完全接受它。
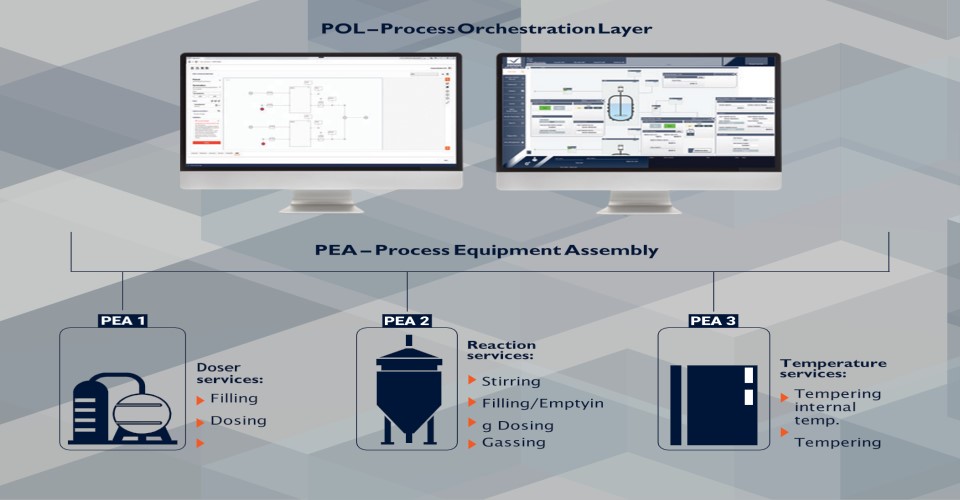
MTP 可以提供帮助的另一个领域是在具有复杂生产线的制造环境中,这类生产线会由来多个不同供应商的设备组成。通过 MTP 应用流程编排层 (POL),我们可以做到最大限度地降低这种复杂性。POL 能在模块化自动化中发挥重要作用,它可以充当控制中心来监督和协调多个任务、系统和工作流程,可以确保端到端作业的顺利进行。编排层位于每个自动化任务之上,其功能被用于充当智能连接器以集成各种系统和应用程序。
Thomas Makait:我同意。MTP 可以轻松适应多种应用场合,无论是应用在连续制造、批次生产企业,或是在带移动端、可互换模块的多品种灵活制造生产平台上。
Giuseppe Menin: Thomas,作为一名量化系统验证(CSV)高级顾问,您认为您所在行业对模块化自动化的需求正在增长吗?制药公司及其设备制造商对这种方法感兴趣吗?
Thomas Makait: 目前整个制药行业对模块化自动化的兴趣肯定在增长。我的客户们对 MTP 都抱有很高的期望。他们认为这是一种有前途的标准化方法,可以帮助减少目前资格和验证所需要的工作量。工程、委托和资格认证这一领域正在经历迭代和技术的转变。年轻工程师正在进入这个行业,新技术不断涌现。旧的资格认证和验证方法和程序已不再适合——这就是 MTP 的可用武之地。
从技术角度来看,标准化意味着对传统思维方式,即“供应商锁定”和制药公司对法规的具体解释的摆脱。与之相反,我们必须转向供应商和制药公司中立的标准化方法。这将使最终用户能够以合规的方式轻松地将自动化设备连接到过程或更高层。具体到鉴定和验证,良好的自动化制造规范(GAMP)5 就是通过智能、模块化自动化方式将使得自动化设备和控制层之间实现更紧密地集成。
最大的挑战来源于对整个计算系统进行设备鉴定和评估,这得采用整体综合方法,以确保多个部门和组织协同工作。我们还需要说服设备供应商接受 MTP,以达到对设备进行预认证和验证的程度,这能加快与模块化工厂的集成过程。
Giuseppe Menin:Rod,您是 ISPE Pharma 4.0 实践社区 (CoP) 的成员。您能告诉我们什么是制药 4.0 吗?您能告诉我们更多关于您在即插即用工作组中领导的 MTP 工作吗?
Rod Hoffman: 从本质上讲,制药业 4.0 其实是将工业 4.0 的原理应用于制药行业。其目标是使制造商能够实现工业物联网所带来的互通和协作优势。制药业 4.0 有几个子类——其中之一是即插即用。这是将“即插即用”的概念应用于制造环境中。其灵感是来自于可将任意品牌的打印机快速连接至任意计算机的同一方式与概念。这不需要任务复杂的技术设置技能,只用我们有 USB 电缆或无线技术——这一切要归功于即插即用。
即插即用工作组的主要目标是确保制药制造环境中的任何自动化设备都可以无缝集成。这意味着要预先验证设备与其他系统集成的能力,而这将大大缩短传统需要鉴定和验证过程相关的漫长交货时间。
通常,工程师会在设备到达之前花费大量时间编写规范。一旦设备进入车间,他们通常最终会花费更多时间来做纠正工作。这就是确保与上层系统的无缝集成至关重要的地方。我们的工作小组专注于解决现有标准中的差异,这些差异会阻碍我们实现这种高水准的无缝集成和协作性。例如,我们研究了 OPC-UA 架构中报警和审计跟踪方面的差异,这些差异阻碍了我们必须满足的一些关键的制药要求。我们制作了一篇论文来提出一个潜在的解决方案,即在 OPC-UA 中引入了新的数据结构,我们现在已将其发展成为制药行业的 MTP 指南。最终,我们确实看到了 MTP 标准的前景,并认定它可以代表范式的改变。
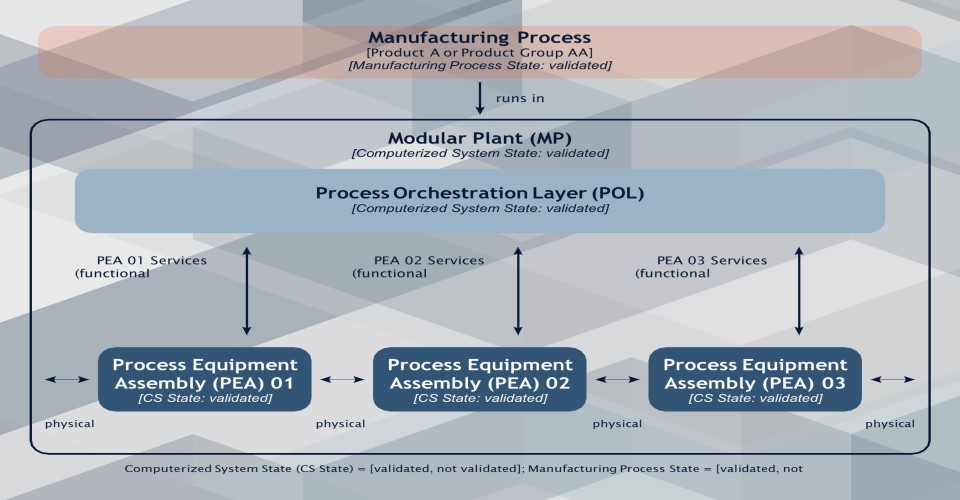
模块化工厂 (MTP) 的运行环境

THOMAS MAKAIT
Thomas Makait 在制药行业拥有超过 25 年的经验,是计算机化系统验证领域经验丰富的顾问。他专门从事验证策略和临时质量管理。他的职业生涯涵盖从赛诺菲的技术合规经理到质量保证经理,在过去的五年里,他一直深入参与模块化工厂工程和 MTP 领域。作为 NAMUR 标准 NE 185 的主要贡献者之一,Thomas 帮助制定了制药行业 MTP 的基本指南,这些指南由活跃的工作组继续制定。
Giuseppe Menin:谁参与了工作组,你们有哪些可交付成果?您认为在制药行业大规模采用 MTP 有什么障碍吗?
Rod Hoffman:我们的工作组是一个非常多元化的团队,由像我这样的行业专家以及供应商的代表组成,包括设备制造商、自动化软件和硬件公司。我们的主要目标是制定指导方针,帮助制药公司在其生产线甚至是在研发实验室环境中采用和实施 MTP。
作为一个团队,我们希望确保所有行业相关者都了解 MTP 的价值。制药公司需要了解 MTP 的价值主张,并要求其供应商支持这种方法。投资者则必须了解它以及它如何使他们受益。目前的冲突在于一些利益相关者仍然不了解这项技术能为他们带来什么,或者更糟糕的是,他们认为这项技术对他们的业务模式构成威胁。
目前我们小组正在为制药行业制定 MTP 实施指南。我们希望通过这个指南为工程师提供生命科学制造业中 MTP 的可能实施场景的概述,包括已经应用 MTP 的实际用例。这应有助于编制要求采用 MTP 的用户要求规范 (URS)。
操作人员可以利用太阳辐射低的时间精确计划维护和清洁工作。这将减少停机时间并提高了系统的整体效率。
Thomas Makait: 一个经常被忽视的方面是制药行业的多样性。它的范围从过程工业应用(例如用于制造活性药物成分 (API))到离散制造应用(例如小瓶和片剂包)。MTP 标准起源于工业行业,对于离散领域来说仍然相对较新,它可能会带来一些额外的障碍。 这是在制药行业实施中期计划时需要考虑的事情。然而,这一点将很快通过将于 2025 年推出的 MTP 2.0 版 (IEC 63280) 标准来弥补。
Giuseppe Menin: Thomas,您是 GAMP DACH 和 GAMP International 的高级成员。您能告诉我们更多关于 GAMP 以及该组织在促进 MTP 方面所发挥的作用吗?
Thomas Makait:早在 2002 年,我就是德国 GAMP DACH 论坛的创始成员之一。虽然当时 GAMP 4 指南已经可用,但将其应用于制药行业的特定应用却是一个挑战。该服务提供商以及设备和 DCS 供应商都需与监管机构密切合作,并参与关于计算机化系统验证的新的创新方法的讨论。
在2020 年,我被受命起草 NAMUR 标准规范在模块化工厂认证的文件,也就是 NAMUR NE 185。在 2022 年我加入了 GAMP DACH 实践论坛时,模块化工厂在制药行业还不是一个热门话题。
然后,我们意识到全球市场对模块化工厂解决方案的需求正在兴起,因此我们创建了一个德国当地的特别兴趣小组(SIG)来满足市场对此的新需求。当时的 SIG 是由来自制药公司的行业专家、设备和系统供应商、系统集成商和专业顾问组成。
Giuseppe Menin:您正在领导国际 GAMP 特别兴趣小组(SIG) “制药模块类型包”,与西门子的 Markus Fink 一起担任联合负责人,专注于模块化工厂的验证。您能告诉我们更多关于这一举措的信息吗?
Thomas Makait:在 2023 年,当时的制药行业对基于 MTP 技术的模块化工厂的需求增加,SIG 被提升到国际层面,以在全球范围内标准化模块化工厂认证和验证的途径。这些活动受到制药行业基于MTP的模块化工厂实施的早期采用者的欢迎和支持。
Giuseppe Menin:如果没有一致的验证框架,模块化工厂概念很难在 GAMP 监管的环境中应用。您领导的 SIG 是如何应对这一挑战的?
Thomas Makait: 我们正经历着激动人心的时代。我本人一直从事自动化行业的工作有近 35 年了。对于我们能有标准将自动化设备与更高级别的自动化系统无缝连接和集成来说这是第一次。现在这种标准化也必须适用于资格认证和验证过程,这是很自然的。我们的目标就是开发基于标准化术语和技术的标准化方法,最大限度地减少模块化工厂合规性鉴定和验证方面的歧义。
一种有希望的方法是定义标准,允许利用供应商模块鉴定、以合规的方式加快现场鉴定和验证。我们需要弥合现有工程项目数据与手动将此类数据传输到模块化工厂鉴定和验证所需的信息之间的差异。参与设备和模块化工厂生命周期的所有企业都面临的主要挑战是涉及多个部门的、利益相关者和组织的。我们的最终目标是使供应商能够合规地提供经过预审和预验证的自动化模块 (PEA)。这是“ISPE GAMP 指南模块化工厂验证和鉴定”的核心,该指南是 Rod 在制药团队内开发的 MTP 4.0 即插即用工作组实施指南的
配套指南。这两份指南都将于 2025 年推出。

GIUSEPPE MENIN
Giuseppe Menin 是工业 4.0 和工业物联网爱好者,在机电一体化、自动化、软件开发和系统集成方面拥有丰富的技术经验 。Giuseppe 于 2004 年加入 COPA-DATA, 目前担任生命科学和过程工业总监。自2014年起,他一直是国际制药工程学会 (ISPE)成员。同时也是 ISPE Pharma 4.0 CoP 和 GAMP 意大利指导委员会的成员。
Giuseppe Menin:在模块化工厂验证的主要领域有哪些可以成功应用 MTP?
Thomas Makait: 模块化工厂布置已经在研究实验室、工艺开发和验证设施中取得了成功。下一步是将这些概念扩展到生产环境,这意味着需要有一个合格的模块化和非模组基础设施,具有固定和移动模块化工艺单元(PEA)的匹配接口。换句话说,我们需要达到这样一个条件,即一旦临床研究完成,相同的模块就可以无缝地转移到生产环境中,为下一个产品的开发腾出空间。
自动化平台的验证策略必须能够将传统的自动化设备与支持 MTP 的自动化集成在一起,因为我们知道大多数自动化设备供应商尚未准备好 MTP。作为先行者,制药公司处于开发这一新市场的最前沿,支持模块供应商开发所需的能力,为生命科学行业提供经过预审和预验证的模块。
有效的标准将加速向模块化的转变
截至今天,工业过程的模块化设备设计不仅在学术界进行讨论,而且还在工业应用中进行了测试。这些创新的智能制造工厂旨在提供必要的灵活性,使生产商能够合规地快速响应不断变化的市场条件。
MTP 已被证明是可以支持模块化制造概念的标准。现在需要将这一概念转化为整个行业的最佳实践。我们还需要考虑智能制造集成以及资格预审和预验证请求,作为购买自动化设备时要求的组成部分。
在这一领域,ISPE Pharma 4.0 的 MTP4 ISPE 工作组通过其目前正在开发的文件,旨在为工程师在 URS 的起草阶段提供支持。同样,GAMP 在制药 SIG 中的 MTP 通过“ISPE GAMP 指南模块化工厂验证和鉴定”文件旨在支持从事设备鉴定和计算系统验证活动的工程师。这些努力将是迈向基于模块化和可协作的制造工厂和平台的智能制造的关键一步。